合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
LB膜分析仪应用:不同初始表面压力条件对VhPLD的磷脂吸附亲和力影响(一)
来源:中国油脂 浏览 873 次 发布时间:2024-07-03
磷脂酶D(Phospholipase D,PLD)(EC 3.1.4.4)是一类能水解磷脂质生成磷脂酸和羟基化合物的酶[1]。除了具有水解活性外,PLD还可通过磷酰基转移作用催化磷脂质极性头部基团的转移反应,从而将大量磷脂酰胆碱(PC)催化合成为自然界稀有的磷脂质,如磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)等[2-3]。合成的磷脂质在食品、化妆品、药品中具有重要应用价值[1]。目前,磷脂酶D已成为合成和改造磷脂质的重要工具[1]。从催化反应过程看,无论是催化磷脂质水解反应还是磷酰基转移反应,由于磷脂酶D的反应底物是不溶于水的磷脂,因此与脂肪酶类似,磷脂酶D也属于界面酶。界面酶催化水解反应的进程大致可分为两步,首先水中游离的酶蛋白在脂质底物存在的条件下,从水相聚集到“脂质-水界面”上。其次,脂质底物进入酶蛋白催化活性中心,发生相应的催化反应,生成目的产物[4]。已有研究表明,“磷脂质-水界面”的存在以及界面的质量对于磷脂酶D活力的充分发挥具有重要影响[5]。而界面吸附作为酶催化反应的首要步骤,在该过程中发挥着重要作用。但目前对于磷脂酶D而言,大部分研究集中在利用其进行特定结构磷脂的合成[3],对于酶蛋白对脂质界面吸附特性的研究鲜有报道。
来源于哈维氏弧菌的磷脂酶D是新发现的一种酶,目前对于该酶的酶学特性尤其是该酶对不同磷脂底物的吸附动力学尚未见有相关报道。单分子层膜是目前公认的研究酶蛋白与脂质相互作用的经典模型[6]。基于单分子层技术可实现脂质单分子层-水界面特性的精准控制,从而为分子水平研究酶蛋白在磷脂质-水界面上的吸附动力学奠定基础[7-9]。本研究首次利用单分子层技术研究该酶对不同磷脂底物的吸附动力学,以期深入了解该酶的界面吸附特性以及针对该酶进行开发与应用。
1材料与方法
1.1实验材料
1.1.1原料与试剂
L-α-磷脂酰胆碱(≥97%)、L-α-磷脂酰肌醇(≥99%),L-α-磷脂酰丝氨酸(≥97%),L-α-磷脂酰乙醇胺(≥99%),L-α-磷脂酰甘油(≥98%),均购于Sigma公司;氨苄抗生素、pET21a表达载体、诱导剂IPTG,均购于Invitrogen公司;质粒提取试剂盒、BCA蛋白定量试剂盒,购于上海生工生物工程有限公司。其他试剂均为分析纯。
1.1.2仪器与设备
葡聚糖凝胶G-25柱(1 000~5 000 Da,1 cm×20 cm,GEHealthcare Bio-Science AB),Q柱(5 mL预装柱,嫁接葡聚糖的Seplite 6FF,配体—CH2N+(CH3)Cl-,粒径50~150μm,流速300~500 cm/h,工作温度4~40℃,pH范围2~12,储存缓冲液20%乙醇,温度4~8℃),HYG-C型恒温振荡培养箱,JY92-IIN超声破碎仪,Biologic LP蛋白层析仪(Bio-Rad公司),ELx800酶标仪(BioTek公司),Micro TroughX LB膜分析仪(配备有界面吸附专用反应槽,芬兰Kibron公司),DTCZ-240N SDS-PAGE电泳仪,Triple TOF 5600 LC-MS质谱仪(美国AB SCIEX公司)。
1.2实验方法
1.2.1失活型哈维氏弧菌磷脂酶D大肠杆菌重组表达菌株的构建
首先,从NCBI蛋白数据库中下载哈维氏弧菌磷脂酶D的完整蛋白序列(GenBank:WP_005435673.1)。用在线信号肽分析软件SignalP 4.1 server对其信号肽进行分析预测。去掉N端24个信号肽氨基酸后的蛋白序列称为成熟蛋白序列。编码磷脂酶D成熟蛋白(VhPLD)的基因序列委托上海生工生物工程有限公司参照大肠杆菌密码子偏好性进行优化,同时在优化的基因序列N端和C端分别添加NdeI和XhoI酶切位点并进行全基因序列的合成。合成的VhPLD基因用NdeI和XhoI内切酶酶切后连入用相同内切酶进行酶切的pET21a表达载体。将构建的质粒pET21a-VhPLD转化大肠杆菌DH 5α感受态细胞并进行测序验证。为了避免酶水解磷脂从而对酶蛋白的吸附过程研究造成干扰,在已经构建的pET21a-VhPLD表达载体的基础上进一步引入针对催化活性位点His157的单点突变(H157A),从而使表达酶蛋白丧失水解活性。单点突变体的构建采用重叠延伸法进行。将构建的突变体pET21a-VhPLD-H157A转化大肠杆菌DH 5α感受态细胞并进行测序验证。将测序正确的质粒进一步转化到E.coliShuffleT7感受态细胞中,阳性克隆鉴定成功后,获得失活型哈维氏弧菌磷脂酶D的大肠杆菌重组表达菌株。
1.2.2失活型VhPLD的表达与纯化
将重组表达菌株接种于5 mL含有氨苄抗生素的LB液体培养基(0.5%酵母提取物,1%蛋白胨,1%NaCl)中,37℃下过夜培养,制备种子液。按5%接种量接种放大于含有氨苄抗生素的LB液体培养基中,37℃、200 r/min下培养2~3 h至OD600为0.6~0.8,加入诱导剂IPTG,至终浓度为0.05 mmol/L。调整培养温度到20℃,继续发酵培养24 h。将诱导表达后的发酵菌液离心(8 000 r/min,6 min,4℃),去上清液,菌体用50 mmol/L Tris-HCl、100 mmol/L NaCl(pH 8.0)重悬,超声破碎15 min,离心(10 000 r/min,15 min,4℃),收集破碎上清,用0.45μm滤膜过滤。将收集到的破碎上清液进行Ni2+亲和层析。蛋白上样后,用Buffer A(50 mmol/L Tris-HCl,100 mmol/L NaCl,pH 8.0)冲洗,紧接着用Buffer B(含有100~500 mmol/L咪唑的Buffer A)进行梯度洗脱,收集出峰的蛋白样品。将100 mmol/L咪唑梯度洗脱收集的出峰样品用G-25柱脱盐后,上样Q柱阴离子交换层析,最终用含有300 mmol/L氯化钠的缓冲液(50 mmol/L Tris-HCl,pH 8.0)洗脱得到目的蛋白样品。所得到的蛋白样品经SDS-PAGE电泳检测其纯度,用BCA蛋白定量检测试剂盒测定其蛋白浓度,用Triple TOF 5600 LC-MS(AB SCIEX)质谱仪进行LC-MS/MS鉴定分析。
1.2.3 VhPLD对不同磷脂单分子层吸附动力学参数测定
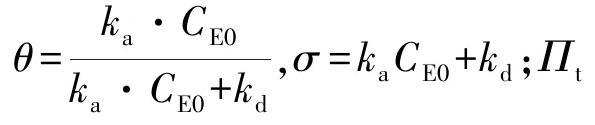
2结果与讨论
2.1失活型哈维氏弧菌磷脂酶D的表达与纯化
大肠杆菌表达系统相比于酵母表达系统,具有发酵周期短的优势。考虑到所表达目的蛋白来源于哈维氏弧菌这一原核细胞,因此在构建VhPLD重组表达体系的选择上,大肠杆菌表达系统成为本研究的首选。诱导表达后的电泳结果表明,虽然有部分目的蛋白以包涵体的形式存在于菌体破碎后的离心沉淀中,但破碎上清液中仍有部分可溶性蛋白存在。将破碎细胞上清液首先采用Ni2+亲和层析纯化,目的蛋白在含有100 mmol/L咪唑的Buffer A洗脱峰样品中得以富集。洗脱峰样品用G25柱脱盐去除所含有的咪唑后,用Q柱阴离子交换层析对样品作进一步纯化。目的蛋白用含有300 mmol/L氯化钠的50 mmol/L Tris-HCl(pH 8.0)洗脱缓冲液洗脱。电泳结果(如图1)表明,在54 kDa左右处有明显的条带,蛋白大小与预期的结果类似(预测理论相对分子质量53 450.65 Da)。同时,取该蛋白条带用Triple TOF 5600 LC-MS(AB SCIEX)质谱仪进行LC-MS/MS分析鉴定,确认该条带即为要表达的目的蛋白。
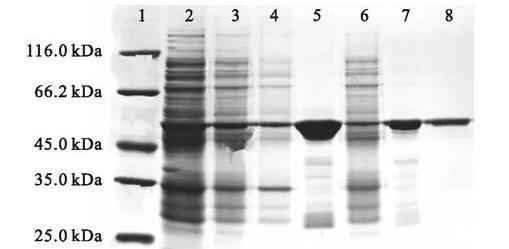
图1失活型VhPLD的表达与纯化SDS-PAGE电泳图注:1.蛋白marker;2.菌体破碎液;3.菌体破碎后离心所得上清液;4.菌体破碎后离心所得沉淀;5.镍柱纯化所得100 mmol/L咪唑洗脱峰样品;6.镍柱纯化的上样穿过峰样品;7.G-25柱纯化的洗脱峰样品;8.Q柱纯化的300 mmol/L氯化钠梯度洗脱峰样品。










