合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
-
> 新工艺提升叶黄素和玉米黄素联产的塔式萃取效率
> 电极界面剩余电荷量越大,界面张力(界面自由能)就越小
> 纳米沸石咪唑酯骨架ZIF-8颗粒的油水界面张力和接触角测定及岩心驱替实验——摘要、材料与方法
> 界面张力为22mN/m的柴油-水分离滤纸振动特性研究(二)
> 微凝胶颗粒在气液界面处吸附动力学及动态方程研究——结果和讨论、结论、致谢!
> 面向高效环保灭火剂的界面张力最小化:短链氟碳复配体系的设计与解析(一)
> 烧结矿致密化行为研究:不同碱度条件下熔体的表面张力、表观黏度值(二)
> 旋转液滴法测量和计算界面张力的方法
> 烧结矿致密化行为研究:不同碱度条件下熔体的表面张力、表观黏度值(三)
> 手机实验软件测量液体表面张力系数VS传统实验效果比较
仲醇聚氧乙烯醚硫酸盐平衡和动态表面张力及应用性能研究(二)
来源:中国洗涤用品工业 浏览 1184 次 发布时间:2024-10-24
2结果与讨论
2.1光学微流变分析
微流变可以通过跟踪粒子的布朗运动获得均方位移(mean square displacement,MSD)值测量样品的黏弹性特性。从图1中可以看出,随着样品老化时间的增加,SAES和AES的MSD曲线都是首先由长位移向短位移转变,即弹性增加,粒子间碰撞增加;去相关时间由短向长的MSD曲线变化,表明二者的黏度增加。SAES和AES在样品老化过程中,其结构都发生了变化,黏弹性都有所增加。从图1中还可以看出,SAES和AES的黏弹性差别较大,在老化过程中SAES黏弹性变化较小,而AES的黏弹性变化较大。
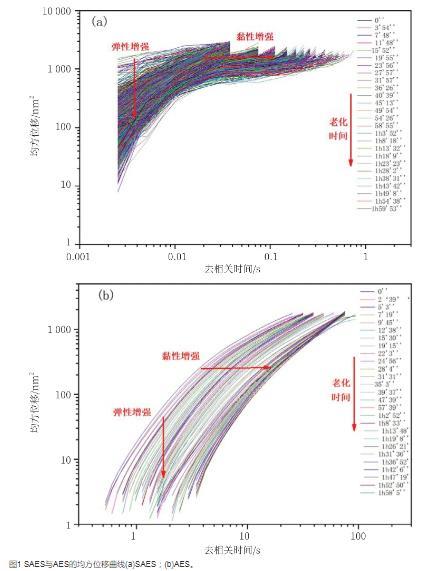
图1 SAES与AES的均方位移曲线(a)SAES;(b)AES。
图2(a)为SAES和AES的弹性因子(EI)随时间变化曲线。从图中可以看出,随着时间的增加,AES的弹性因子逐渐增大,说明在样品放置过程中其结构明显增强;而SAES的弹性因子基本不发生变化,说明在样品放置过程中其结构基本不发生变化。这可能是因为AES的亲水基SO4-基团位于碳氢链的端点,而SAES的SO4-基团位于疏水链的中间位置,相比AES,SAES结构中存在支链,粒子间相互作用较差。AES的最终弹性因子为1.77×10-2nm-2,明显高于SAES的最终弹性因子9.10×10-4nm-2。
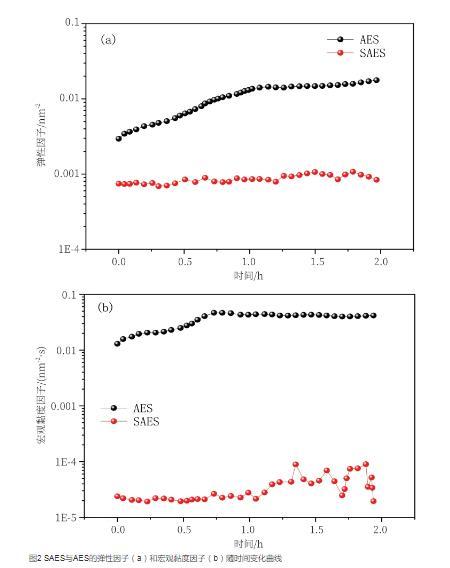
图2 SAES与AES的弹性因子(a)和宏观黏度因子(b)随时间变化曲线
图2(b)为SAES和AES的宏观黏度因子(MVI)随时间变化曲线。粒子移动到一定距离的时间越长,表示液滴运动速度越低,MVI值越高,相应地样品的黏度越高,体系的结构越强。从图中可以看出,随着时间的增加,SAES和AES的宏观黏度因子都有所增加,但增加的幅度不大。AES的最终宏观黏度因子为4.21×10-2nm-2·s,远远高于SAES的最终宏观黏度因子6.91×10-5nm-2·s。在实际应用过程中,黏度更低的SAES使用更为方便。
2.2表面张力
2.2.1平衡表面张力
图3为SAES和AES水溶液的表面张力随浓度变化曲线。从图中可以看出,随着SAES和AES水溶液浓度的增加,表面张力都逐渐降低,这意味着在界面上开始出现紧密排列,到达cmc以后,表面张力不再变化,为一常数,说明在体相内已经形成了聚集体。根据公式1和公式2可以得出表面活性剂在气液界面的饱和吸附量Гmax和最小分子截面积Amin。根据Dahanayake等提出的吸附效率pC20的物理意义,即得溶剂表面张力降低20 mN/m时所需表面活性剂浓度的负对数,根据公式3可以计算出表面活性剂的pc20值。pc20是度量表面活性剂表面活性的一个重要参数,其值越高说明表面活性剂的吸附效率越高。
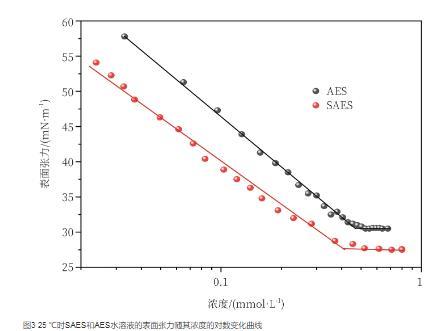
图3 25℃时SAES和AES水溶液的表面张力随其浓度的对数变化曲线
式中n是一个常数,对于1∶1型离子型表面活性剂,其在水溶液中以表面活性离子和反离子的形式存在,根据电中性原则,正离子与负离子的吸附量相等,式中n=2。R为气体常数8.314 J/(mol·K),T为绝对温度K,NA为阿伏伽德罗常数6.02×1023,C20为当水的表面张力降低20 mN/m时所需表面活性剂的浓度。由表面张力曲线得到AES和SAES的表面性质相关数据如表1所示。从表1可以看出,AES溶液的cmc和γcmc分别为0.45 mmol/L和30.77 mN/m,该值与文献报道的AES的cmc(0.33 mmol/L)和γcmc(33~34 mN/m)数值接近。SAES的cmc和γcmc分别为0.42 mmol/L和27.71 mN/m。SAES和AES的cmc值基本一致,这可能是由于二者具有相同的碳原子数,分子之间的疏水相互作用基本相同所致。相比AES,SAES由于支化结构的存在,增加了表面活性剂分子在水表面的覆盖率,从而使γcmc有所降低。这与一些文献报道的支链型表面活性剂降低表面张力的能力优于直链型的结果相一致。支链化的结构也使其Amin增大,Гmax减小。

表1 25℃时SAES和AES的表面活性参数
2.2.2动态表面张力
对某一浓度表面活性剂溶液,达到吸附平衡前某一时刻的表面张力称为动态表面张力(dynamic surface tension,DST),在某些体系中动态表面张力比平衡表面张力更重要。如在涂膜过程中,新表面不断形成,若表面张力降低速度缓慢,就会导致涂布不均匀等。因此研究表面张力随时间的变化具有十分重要的意义。本实验通过最大泡压法分别测定了25℃下两种表面活性剂在水溶液中的吸附行为。结果如图4所示。

图4 25℃时不同浓度的SAES和AES水溶液的动态表面张力(a)SAES;(b)AES。
从图4可以看出所测不同浓度不同表面活性剂的表面张力在初始阶段均快速下降,一定时间后趋于平稳状态。这是因为动态表面张力测试过程中新形成的表面远偏离于平衡态,吸附层离子的浓度很低,体相与吸附层的浓度差大,因此动态表面张力变化很大。随着吸附的进行,次表面浓度和表面浓度逐渐增大,扩散和吸附的速度均逐渐降低,动态表面张力随着吸附时间的增加而降低的趋势也逐渐变得平缓。当表面活性剂浓度增大时,表面张力的下降幅度和速度也随之增大,而且相应地缩短了到达平衡状态的时间。这种随体系浓度的增加达到平衡所需的时间越短的趋势与已经报道的一些烷基表面活性剂的结果是相一致的。在相同浓度下,SAES表面张力下降的速率大于AES,这是由于SO4-在碳氢链中间的化合物比在端点者扩散速度快。
当溶液浓度较小时,可以采用Ward-Tordai方程来描述溶液体相与次表面之间的传质过程:
从该公式中可以看出后一项含有卷积积分,使此方程不可解。
当t→0时,属于短时吸附过程,由公式4可转化为公式5:
式中,γt指时间t时的表面张力(mN/m);γ0为去离子水的表面张力(mN/m);SAES和AES为1∶1型阴离子表面活性剂,则n=2,Ds为短时吸附过程的扩散系数(m2/s);R为气体常数8.314 J/(mol·K),T为绝对温度K。
当t→∞时,此过程属于长时吸附过程,可由公式4转化为公式6:
结合Gibbs方程,可演变成公式7:
式中,γeq为t→∞时的表面张力(mN/m);Г为表面过剩量;Гeq为平衡表面过剩量;Dl为长时吸附过程的扩散系数(m2/s)。
图5和图6分别为不同浓度的SAES溶液和AES溶液的γt随t1/2与t-1/2的变化曲线图。分别对其进行拟合,当t→0时,γt与t1/2呈直线关系,直线的截距为溶剂水的表面张力;当t→∞时,γt与t-1/2也呈直线关系,直线的截距为不同浓度下表面活性剂水溶液的平衡表面张力。通过求直线部分的斜率可以得出Ds、Dl值及相应的比值。结果列于表2中。由表2可以看出,随浓度的增加,Ds与Dl均减小,这是因为随着浓度的增大,分子间静电斥力作用增大,从而使得分子的自由运动受到限制。通过比较SAES和AES的Ds值可以发现,SAES的Ds值均大于AES,说明SAES在吸附初期的吸附扩散速率较快;SAES的Dl值均小于AES,说明SAES在吸附后期由于空间位阻等的效应使得吸附势垒更高。Ds与Dl的比值远小于1,这意味着Ds与Dl差别比较大,说明吸附后期为混合动力控制吸附。
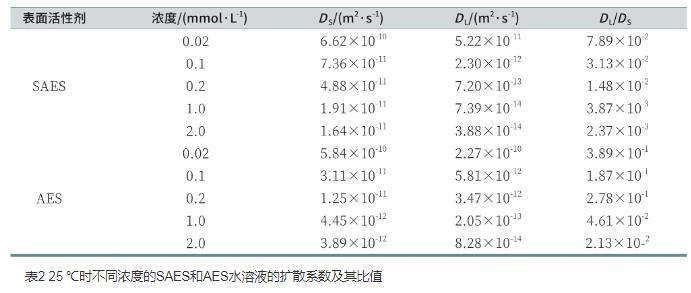
表2 25℃时不同浓度的SAES和AES水溶液的扩散系数及其比值
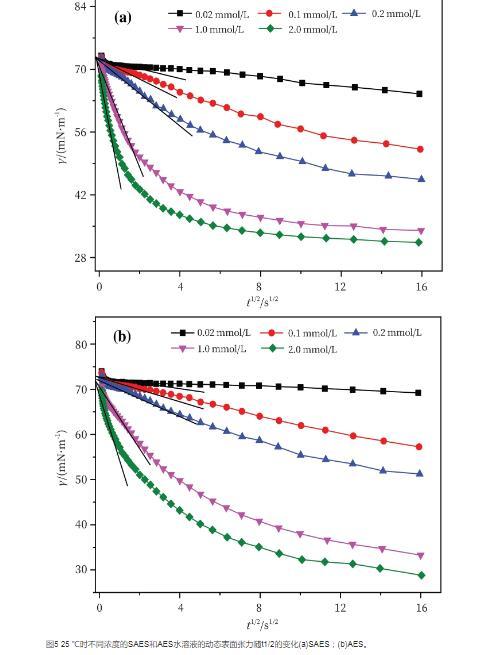
图5 25℃时不同浓度的SAES和AES水溶液的动态表面张力随t1/2的变化(a)SAES;(b)AES。
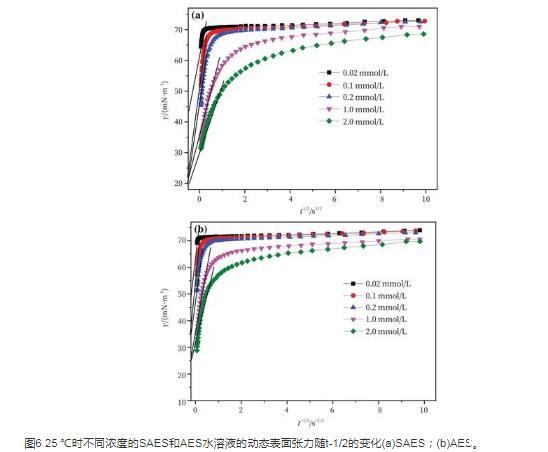
图6 25℃时不同浓度的SAES和AES水溶液的动态表面张力随t-1/2的变化(a)SAES;(b)AES。










